近年、化粧品の安全性に対する消費者の意識が高まる中で、製造現場における品質管理の重要性がかつてないほど増しています。
「自社の製品品質をより確実に保証したい」「海外への輸出を視野に入れている」といった場面で、必ずキーワードとなるのが「化粧品GMP」です。
しかし、いざ取り組もうとしても、「医薬品のGMPと何が違うのか」「法律で義務付けられているのか」「具体的に何をすればよいのか」といった疑問を持つ担当者の方も多いのではないでしょうか。
専門用語が多く、ハードルが高く感じられることも、取り組みを躊躇させる要因の一つです。
この記事では、化粧品GMPの基礎知識からISO22716との関係、現場で徹底すべき3原則、そして具体的な導入メリットまでをわかりやすく解説します。
読み終わる頃には、自社がどのようなステップでGMP体制を構築すべきかの道筋が明確になるはずです。
化粧品OEMメーカーのホシケミカルズが提供する製品は「スターラボ・グループ」という国内外5カ所の製造拠点を含めた組織で連携し、開発・製造を進めています。
グループの中で、主にスキンケア製品の製造を担うオーラコスメティックス工場(群馬/スキンケア・ヘアケア)では、2004年4月ISO9001を取得、2018年4月に化粧品GMP(ISO22716)への切り替えを実施しました。
エステノーバ工場(埼玉/スキンケア・ヘアケア)でも、2014年4月にISO9001取得、2018年7月にISO22716(化粧品GMP)への切り替えを実施しています。
化粧品GMPとはどのような基準なのか?
 化粧品製造の現場において、品質と安全性を確保するために設けられた基準が「化粧品GMP」です。
化粧品製造の現場において、品質と安全性を確保するために設けられた基準が「化粧品GMP」です。
GMPとは「Good Manufacturing Practice」の略称で、日本語では「適正製造規範」と訳されます。
製品が出荷されるまでの全工程において、「誰がいつ作っても、同じ品質の製品ができること」を担保するための仕組みと言えます。
まずは、この基準がどのような背景で生まれ、日本の法律や国際規格とどう関わっているのかを整理していきましょう。
ISO22716との関係と位置づけ
現在、日本で一般的に「化粧品GMP」と呼ばれるものは、国際規格である「ISO22716」を指すことがほとんどです。
ISO22716は、化粧品の製造および品質管理に関するガイドラインとして、国際標準化機構(ISO)によって2007年に発行されました。
日本においては、日本化粧品工業連合会(粧工連)がこのISO22716を採用し、業界の自主基準として運用しています。
つまり、日本国内の化粧品GMPは、世界共通のグローバルスタンダードと整合性が取られているということです。
これにより、日本で作られた化粧品が海外でも品質面で信頼される土壌が整っています。
医薬品GMPとの決定的な違い
よく混同されがちなのが「医薬品GMP」との違いです。
両者は目的こそ「品質の確保」で共通していますが、その強制力と管理の厳格さに大きな差があります。
医薬品GMPは、薬機法に基づく「省令」であり、遵守しなければ製造許可が下りないかつ、品目ごとの承認が得られない法的義務です。
人の生命や健康に直接影響を与える医薬品を扱うため、極めて厳格なバリデーション(検証)や文書管理が求められます。
一方、化粧品GMPは、製造工程の管理や衛生管理を求める点では同じですが、基本的には「自主基準」の枠組みです。
製品リスクが医薬品に比べて相対的に低いことなどから、各企業の裁量に委ねられる部分が残されています。
【関連記事】化粧品OEMお役立ち情報 | ②化粧品OEMと化粧品ODMの違い

日本における法的拘束力の有無
前述の通り、現時点での日本では、化粧品GMPの遵守は法律による「義務」ではありません。
遵守しなかったからといって、直ちに違法となり営業停止になるわけではないのです。
しかし、だからといって「やらなくていい」と判断するのは品質や信頼性の観点から推奨されません。
薬機法では、製造販売業者に対してGQP省令(化粧品の品質管理の基準医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準)の遵守を求めています。
このGQPを適切に運用するためには、製造所(工場)が適切な製造管理を行っていることが大前提となります。
厚生労働省や都道府県の薬務課も、実地調査の際には化粧品GMP(ISO22716)のガイドラインを参考にするケースも想定されます。
事実上、GMPに準拠した管理体制は、化粧品ビジネスを継続するための「必須要件」になりつつあると言えるでしょう。
現場で守るべき化粧品GMPの3原則とは?
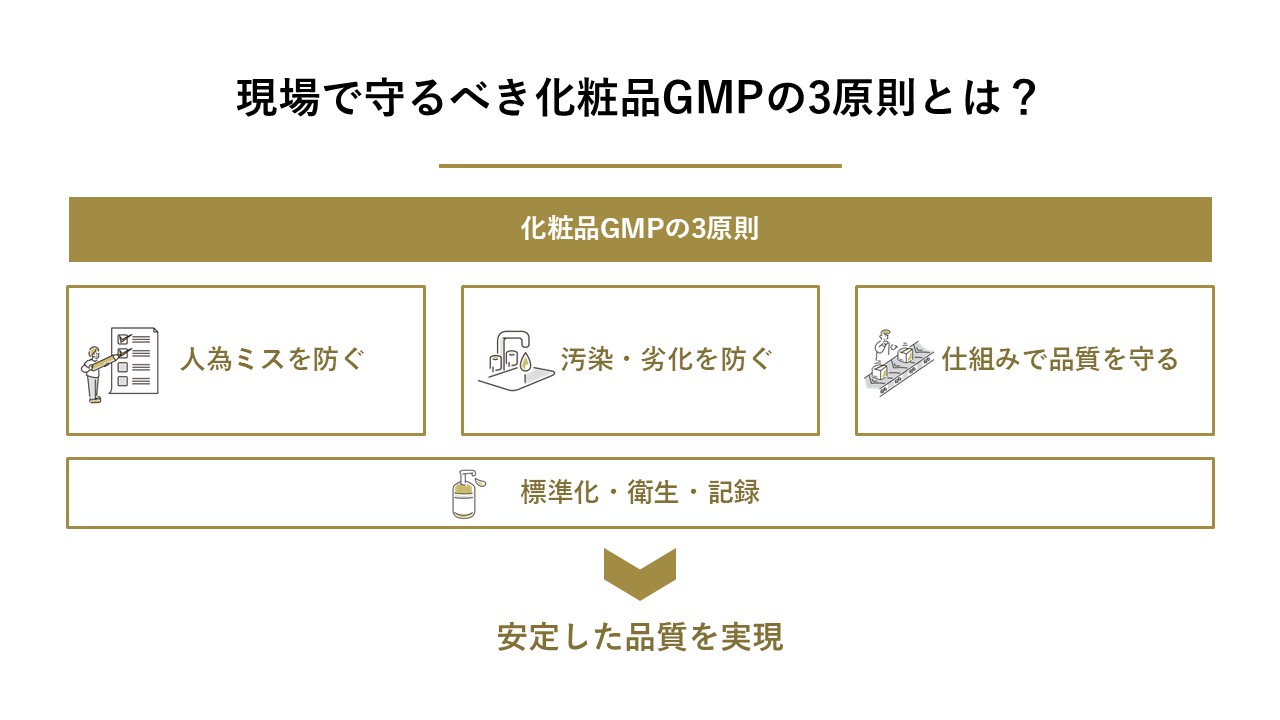 化粧品GMPには、膨大なルールやチェック項目が存在しますが、それらすべての根底には共通する3つの考え方があります。
化粧品GMPには、膨大なルールやチェック項目が存在しますが、それらすべての根底には共通する3つの考え方があります。
これを「GMPの3原則」と呼びます。
細かい手順書を作る前に、まずはこの3原則を現場の全員が理解しておくことが重要です。
すべてのルールは、この3つの目的のいずれかを達成するために存在しているからです。
人為的なミスを最小限にする
製造現場で最も起こりやすいトラブルの原因は「人」です。
原料の取り違え、計量(秤量)ミス、ラベルの貼り間違いなど、ヒューマンエラーはいつでも起こり得ます。
これを防ぐために、GMPでは「作業の標準化」を徹底します。
口頭での指示を禁止し、すべて文書化された手順書に基づいて作業を行うことや、重要工程でのダブルチェック(二人一組での確認)などが具体的な対策となります。
誰が担当しても同じ結果が出せるように、人の記憶や勘に頼らない仕組みを作ることが第一の原則です。

オーラコスメティクス工場では、処方に基づく緻密な計量が求められる「原料の秤量」という工程に独自の「秤量・製造管理システム」を導入し、ヒューマンエラー対策を徹底しています。
原料ごとにQRコードを付与し在庫管理を行うことで、過不足や誤使用があった場合はアラートが表示され未然に人的ミスを防ぎます。配合量がわずかに変わるだけでも、最終製品の粘度・香り・色などに影響するため、秤量は正確性が求められる作業です。
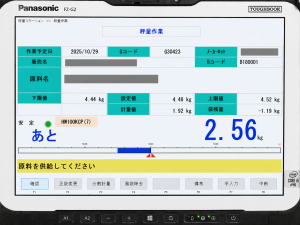
秤量作業タブレット画面イメージ
汚染および品質低下を防ぐ
化粧品は肌に直接触れるものであり、微生物による汚染や異物混入は絶対にあってはなりません。
また、時間の経過とともに成分が変質することも防ぐ必要があります。
この原則に基づき、製造設備や作業環境の衛生管理(清掃・消毒)が厳しく求められます。
例えば、虫や埃が入らないような空調設備の導入、作業員の服装や手洗いの徹底、交差汚染(異なる製品の成分が混ざること)を防ぐための動線確保などがこれに当たります。
製品が置かれる環境そのものを清潔かつ適切に保つことが求められます。
オーラコスメティックス工場では、非常に厳しい「衛生管理基準」に基づいた「クリーンルーム」が設けられています。
ここでは、敏感肌用の化粧品などが製造されています。
衛生管理機器の一例
プラズマクラスター搭載エアシャワー
プラズマクラスターイオン搭載による静電気抑制効果で、目に見えない微粒子など、異物除去性能が向上。
さらに異物の再付着も抑制します。
クリーンセル(ヘパフィルター)
充填室を陽圧状態に保ち、クリーンな空気が室内に入ってくる仕組みです。
0.2ミクロンほどの小さな埃なども取り除きます。
静電気除去装置
容器などのプラスチック製品が多く、静電気が発生しやすい環境です。
自動車工場の塗装ラインにも導入されている装置で、空気中の落下菌まで除去。


8S運動啓発ポスター
当グループでは、「8S運動」という独自の取り組みを実施しています。
「8S」は、整理・整頓・清掃・清潔・しつけ・SAFETY・SAVE・SMILEを表します。
特に最後のSMILEは、仲間同士が協力しあう環境づくりに大きな役割を担っています。
高品質を保証するシステム設計
3つ目は、個人の努力ではなく「組織としての仕組み(システム)」で品質を保証することです。
これは、製造部門だけでなく、品質管理部門が独立した権限(※1)を持ち、客観的に製品の合否を判定する体制を指します。
万が一、市場でトラブルが起きた際に、すぐに原因を特定できるトレーサビリティ(追跡可能性)(※2)の確保や、定期的な内部監査による自己点検もこのシステムに含まれます。「ミスが起きないように祈る」のではなく、「ミスが起こることを防ぎ、ミスが起きてもすぐに検知し、改善できる仕組み」を構築することが、高い品質保証には不可欠です。
【関連記事】化粧品OEMお役立ち情報 | ⑨商品開発における“環境に配慮”した取り組み

これにより、トレーサビリティの追跡はもちろん、計量時のダブルチェック・トリプルチェックの廃止や、棚卸作業の簡略化、類似原料の誤使用防止など様々なメリットも生まれています。
具体的に満たすべき17の要求事項とは?
 ISO22716(化粧品GMP)では、製造管理と品質管理に関して、具体的に17のセクション(要求事項)を定めています。
ISO22716(化粧品GMP)では、製造管理と品質管理に関して、具体的に17のセクション(要求事項)を定めています。
そのセクションは、適用範囲・用語及び定義・従業員・構造設備・機器・原料及び包装材料・生産・最終製品・品質管理試験室・規格外品の処理・廃棄物・委託・逸脱・苦情及び回収・変更管理・内部監査・文書化といった事項です。
これらは大きく分けると、建物や機械などの「ハード面」と、人やルールなどの「ソフト面」に分類できます。
それぞれの要素がどのように関わっているのか、以下の表で整理します。
| 分類 | 主な要求事項(セクション) | 具体的な管理内容の例 |
| ハード面 | 構造設備、機器、品質管理試験室 | ・清掃・消毒が容易な材質の床や壁・防虫防鼠(ぼうそ)対策が施された施設・定期的な校正・メンテナンスが行われている製造機器 |
| ソフト面 | 文書化、生産、規格外品の処理 | ・すべての作業手順のSOP(標準作業手順書)作成・製造記録、試験記録の保管・不良品が発生した際の処理ルールの明確化 |
参考:https://www.pref.kyoto.jp/yakumu/documents/kougyoukai.pdf(化粧品GMPガイドラインについて)
ハード面における構造設備の要件
ハード面では、製品を汚染から守るための物理的な環境整備が求められます。
高価な最新設備を入れる必要はありませんが、「清掃しやすく、汚れが溜まらない構造」であることは必須です。
例えば、製造エリアと包装エリアを区分けして粉塵の飛散を防ぐことや、手洗い設備を作業室の入り口に設置することなどが挙げられます。
また、使用する水(製造用水)の品質管理も極めて重要であり、水質検査を定期的に行い、配管内に水が滞留しない設計にするなどの配慮が必要です。
ソフト面における手順書と記録管理
ソフト面の核心は「文書化」です。GMPの世界では「記録のないものは実施していないのと同じ」とみなされます。
まず、原料の受け入れから出荷までの全工程について、「誰が・いつ・何を・どのように」行うかを記した規定と手順書(SOP)を作成します。
そして、実際の作業時には、その手順通りに行ったことを記録に残します。
もし手順から逸脱した場合(例:温度を規定より上げってしまった等)は、その事実と処置内容を正直に記録し、品質への影響を評価するプロセスが不可欠です。

オーラコスメティックス工場では、「記憶に頼るのではなく、記録に頼る」という方針を掲げています。記録を形骸化させないために、現場で本当に役立つフォーマットでの指示書・手順書づくりも追及しています。
組織体制と従業員への教育訓練
どんなに立派な設備とマニュアルがあっても、それを運用するのは「人」です。
そのため、従業員への教育訓練は要求事項の中でも特に重要視されています。
入社時の基礎教育だけでなく、定期的に衛生管理や作業手順に関する研修を行い、その実施記録を残す必要があります。
また、品質保証責任者や製造責任者といったキーパーソンの責任と権限を明確にし、経営層が品質について関与する姿勢を示すことも、組織としての要求事項に含まれます。
オーラコスメティックス工場では、新入社員へ向け化粧品GMPに関する教育訓練を実施しています。認証制度の概要説明はもちろん、菌対策や服装説明など幅広い内容です。
さらに、化粧品GMPへの理解度をはかる取り組みも定期的に実施しています。社内の意識を高めることで、制度が組織により深く定着していくという考えからです。
なぜ化粧品GMPに取り組む必要があるのか?
法的義務ではない化粧品GMPに対し、多くの企業がコストと労力をかけて取り組むのには理由があります。
それは、単なる「ルールの遵守」を超えた、経営上の大きなメリットが存在するからです。
海外展開における実質的な必須条件となる
近年、日本の化粧品メーカーが海外進出するケースが増えていますが、輸出先によって要件は異なります。
EUでは、EU化粧品規則(Regulation No.1223/2009)によりISO22716への準拠が法的義務となっています。
一方、ASEAN諸国では、ISO22716と同等とされるASEAN化粧品GMPへの適合が推奨されていますが、自主運用規定にとどまり、輸入時に適合証明の提示は義務付けられていません。
GMP体制が整っていないと、現地の代理店と契約できなかったり、輸出時の手続きでGMP証明書の発行ができずにつまずいたりするリスクがあります。
グローバル市場で戦うためには、化粧品GMPはもはや「パスポート」のような存在と言えるでしょう。
ホシケミカルズでは、ベトナムやシンガポール、香港、カンボジア、ミャンマーなどアジアのほぼ全域にOEM製品の輸出実績を持ちます。海外の現地企業からOEMを受注することで様々な国々のトレンドやニーズ、規制などをタイムリーに把握し、それらの情報やノウハウを提供するだけでなく、EPA(経済連携協定)など関税制度も活用した国内クライアントの海外進出サポートを強みとしています。
化粧品GMPを取得した工場での製造を行っているからこそ、こうした輸出案件の実績を積み重ねています。
ホシケミカルズの「国際事業」

自主回収リスクを大幅に低減する
化粧品業界で最も恐ろしいリスクの一つが、製品の「自主回収(リコール)」です。
異物混入や成分の配合ミスなどが市場に出た後に発覚すれば、回収コストがかかるだけでなく、長年築き上げたブランドの信頼が一瞬で失墜します。
化粧品GMPを導入し、原材料のチェックから製造、出荷判定までのプロセスを厳格に管理することで、不良品が市場流出するリスクを限りなくゼロに近づけることができます。
これは結果として、損害賠償やブランド毀損といった見えないコストの削減につながります。
OEM選定時の重要な信頼性指標
化粧品の製造を外部に委託する(OEM)場合、委託元(ブランド側)は製造業者の品質管理能力を見極める必要があります。
このとき、化粧品GMP認証を取得しているか、あるいは化粧品GMPに準拠した管理が行われているかが、選定の決定的な指標となります。
ブランド側(製造販売業者)にはGQP省令に基づく品質管理責任がありますが、製造委託先のOEMメーカーが化粧品GMPに基づいてしっかり管理してくれていれば、その責任を果たすことが容易になります。
つまり、化粧品GMP準拠は私たち化粧品OEMメーカーにとっても「選ばれる工場」になるための強力な営業ツールでもあるのです。
認証取得に向けた導入フローはどう進めるか?
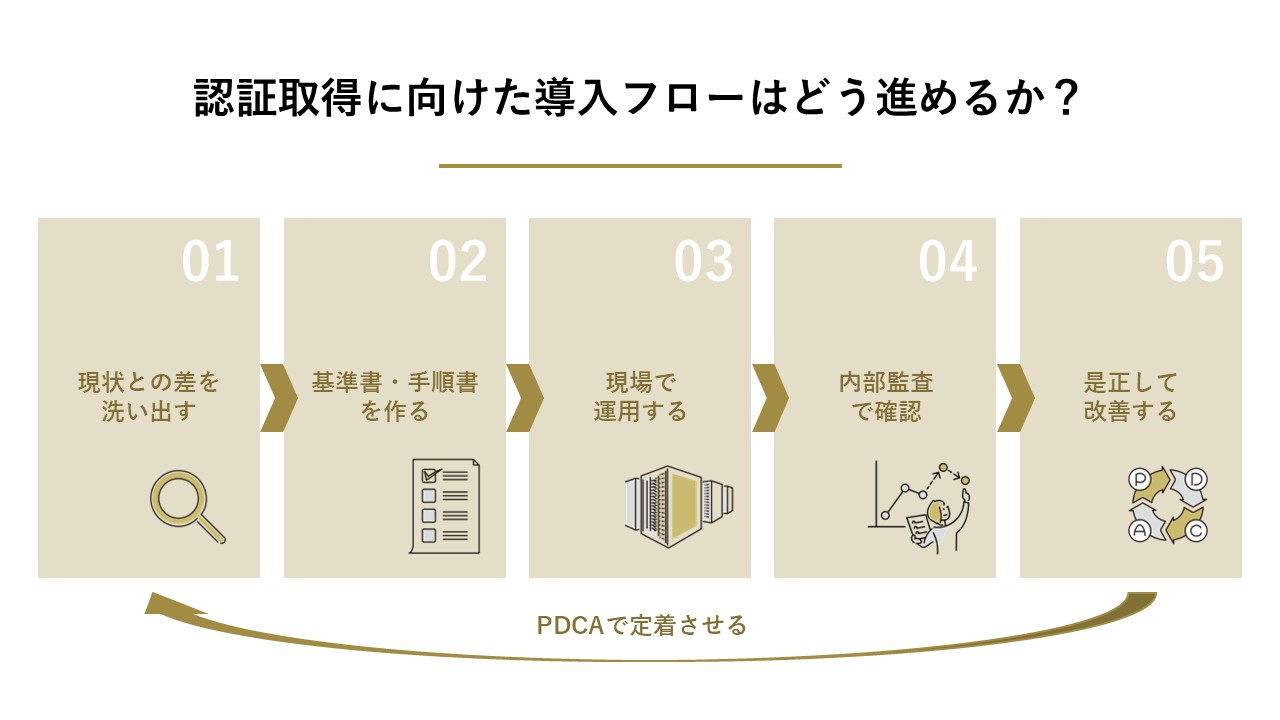 では、実際に化粧品GMPを自社に導入し、認証取得や自己適合宣言(※)を目指す場合、どのように進めればよいのでしょうか。一般的な流れを解説します。
では、実際に化粧品GMPを自社に導入し、認証取得や自己適合宣言(※)を目指す場合、どのように進めればよいのでしょうか。一般的な流れを解説します。
※自己適合宣言とは?
審査機関からの認証を取得せず、工場がISOの要求事項に沿ったマネジメントシステムに則り、導入・運用していることを外向きに宣言することです。
ギャップ分析による現状課題の抽出
最初に行うべきは「現状把握」です。
ISO22716の要求事項(17項目)と、自社の現在の設備・ルール・手順を照らし合わせ、どこが不足しているか(ギャップ)を洗い出します。
これを「ギャップ分析」と呼びます。多くの場合、「手順書が文書化されていない」「衛生教育の記録が残っていない」「清掃ルールが曖昧」といった課題が見つかります。
この段階で、設備改修が必要なハード面の課題と、ルール作りで対応できるソフト面の課題を仕分け、優先順位をつけて計画を立てます。
【関連記事】化粧品OEMお役立ち情報 | ⑦商品開発で重要なのは「目的」を見失わないこと


オーラコスメティックス工場・エステノーバ工場では、ISO9001を取得していた背景もあり、そこに化粧品GMP(ISO22716)の範囲を加え、実情に合った内容に見直しを実施しました。
基準書や手順書の作成と運用開始
次に、洗い出した課題を解決するための文書作成に取り掛かります。
製品ごとの規格を定めた「製品標準書」、製造や清掃の手順を定めた「製造管理基準書」「衛生管理基準書」、そして品質検査のルールを定めた「品質管理基準書」などが主要なドキュメントです。
重要なのは、現場の実態とかけ離れた理想的なルールを作らないことです。
現場の作業担当者も巻き込みながら、「守れるルール」を策定し、それを従業員に教育して実際の運用を開始します。
運用しながら不都合があれば、正規の手続きを経てルールを修正(改訂)していきます。

各部門の責任者による基準書と手順書の作成にあたり、実態に即した内容にするとともに、工場内の掲示物はビジュアル化(図・イラスト・写真など)を多用し、形骸化させないための工夫も加えています。
内部監査の実施と継続的な改善
運用が定着してきたら、社内の人間による「内部監査」を行います。
決められたルール通りに作業が行われているか、記録は正しく残されているかをチェックします。
内部監査で見つかった不備は「是正処置」として改善し、再発防止策を講じます。
この「計画(P)→実行(D)→監査(C)→改善(A)」のサイクルを回し続けることこそが、GMP運用の本質です。
一定のレベルに達した段階で、外部の認証機関による審査を受ければ、晴れてGMP認証取得となります。
内部監査員(主任監査員)の任命
オーラコスメティックス工場では、運用の一環として化粧品GMPの理解度をはかるチェックを定期的に実施しています。
内部監査員(主任監査員)の任命には、この理解度チェックをクリアした者であること、さらに各部署の責任者の推薦、管理責任者の指名という規定で選出しています。
この取り組みの副産物として、理解度の点数化が可能になり、スタッフも事前に自分事化して知識を深めたり、次世代の育成やリーダーシップ能力が育つ社内風土づくりにも繋がっています。
まとめ
化粧品GMPについて、その定義から実践的な導入フローまでを解説しました。
この記事の要点をまとめます。
- 化粧品GMPは「ISO22716」に準拠した自主基準であり、法的義務ではないが実質的な必須要件である。
- 「人為的ミスの防止」「汚染防止」「品質保証システム」の3原則を守ることが運用の核となる。
- 導入により、海外展開の円滑化、回収リスクの低減、取引先からの信頼獲得といった経営メリットが得られる。
化粧品GMPへの取り組みは、単にマニュアルを増やすことではありません。
それは「お客様に安心して使い続けてもらえる製品」を作り続けるための、企業の誠実さの証明でもあります。
まずは自社の現状とガイドラインとのギャップを確認し、できるところから一つずつ、品質管理のレベルを上げていくことをお勧めします。
化粧品OEMメーカーを活用したブランド立ち上げや、
弊社では小ロット(基本1,000個~)から製造に対応しており、豊富な実績とノウハウでお客様の理想の化粧品づくりをサポートします。
商品企画から処方開発、薬事申請、製造、販売戦略まで一貫してお手伝いすることも可能です。
まずはお気軽にお問い合わせください。
ホシケミカルズの「化粧品OEM」について詳しく知りたい方はこちら

監修者 : 佐藤 光昭(株式会社スターラボ・ホールディングス 薬事部マネージャー)
 2003年に東京学芸大学A類社会科(小学校教員養成課程)を卒業、2006年3月株式会社オーラコスメティックスに入社し、2021年3月には薬事部マネージャーに就任。現在は、株式会社スターラボ・ホールディングスに所属。
2003年に東京学芸大学A類社会科(小学校教員養成課程)を卒業、2006年3月株式会社オーラコスメティックスに入社し、2021年3月には薬事部マネージャーに就任。現在は、株式会社スターラボ・ホールディングスに所属。
医薬部外品の申請、化粧品の届出、パッケージや広告表示に関する薬事チェック、化粧品/医薬部外品製造販売業・化粧品/医薬部外品製造業の許認可維持管理、行政対応など、製品が消費者の皆様の手に届くまでのあらゆる段階でその専門性を発揮しています。化粧品および医薬部外品業界に深く携わり、多岐にわたる専門知識と実務経験を有しています。
また、ISO22716(化粧品GMP)の管理責任者として、化粧品の製造管理および品質管理の国際基準遵守を徹底し、スターラボ・グループが手掛ける製品の安全性と品質の向上に貢献しています。
■ 本記事の引用・転載について
本記事の引用・転載にあたって事前の承諾は不要ですが、ご利用の際は以下のルールに基づき、クレジットの明記とサイトへのリンクをお願いいたします。
クレジット表記: 「ホシケミカルズ」または「ホシケミカルズ株式会社」
(例:「ホシケミカルズの調査データより」「出典:ホシケミカルズ株式会社」など)リンク先URL: https://www.starlab.co.jp/
掲載連絡: 公開後で構いませんので、お問い合わせフォームよりお知らせいただけますと幸いです。
※記事内容の意図を歪めるような加工、および公序良俗に反する媒体への掲載は固くお断りします。


